Sifat senyawa kovalen antara lain. Titik didih dan titik leleh relatif rendah.
Perhatikan Beberapa Zat Berikut Asam Klorida
Sedangkan non polar tidak larut dalam air melainkan larut dalam pelarut non polar.
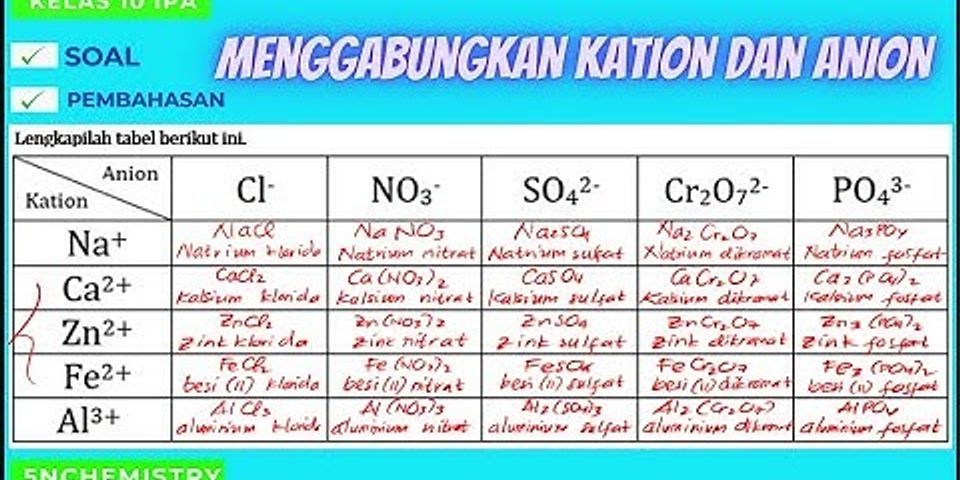
. Senyawa ionik lebih reaktif daripada senyawa molekuler. Senyawa ionik Senyawa ionik adalah senyawa yang atom-atomnya berikatan secara ionik. Titik leleh senyawa ion dan senyawa kovalen memiliki perbedaan yang signifikan.
Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion-ionnya sehingga dapat menghantarkan arus listrik. Perbedaan di atas juga membantu membedakan dan mengidentifikasi apakah senyawa tertentu yang tidak. Sedangkan untuk senyawa kovalen seperti urea dan naftalena tidak dapat menghantarkan arus listrik karena merupakan ikatan kimia dimana terjadi pemakaian elektron secara bersama-sama.
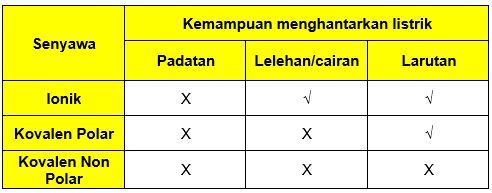
Padatan ionik tiga dimensi ion-ion berikat kuat didalam kisi-kisinya 4Daya Hantar Listrik Dapat menghantarkan listrik ketika berbentuk lelehan. Senyawa ion juga dapat menghantarkan arus listrik bila dilarutkan dalam pelarut polar misalnya air karena terionisasi. 1Senyawa ion memiliki titik didih dan titik leleh yang tinggi 2.
Ion-ion dalam larutan HCl inilah yang berperan sebagai penghantar listrik. KUMPULAN SOAL UN KIMIA DASAR IKATAN KIMIA 1. Wujud senyawa ion yang dapat menghantarkan listrik berupa larutan dan lelehan.
Contoh Soal dan Pembahasan Larutan Senyawa Ionik dan Kovalen. Sehingga kebanyakan senyawa kovalen merupakan nonelektrolit. HCl merupakan senyawa kovalen polar yang berarti mempunyai kutub-kutub positif dan negatif akibat adanya perbedaan keelektronegatifan.
Senyawa ion merupakan zat elektrolit yang kalau larut dalam air hasilnya adalah ion-ion contohnya NaCl dan garam lainnya. NaCl natrium klorida. Banyak perbedaan yang dapat dicatat antara senyawa ionik dan kovalen berdasarkan sifat makroskopiknya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih.
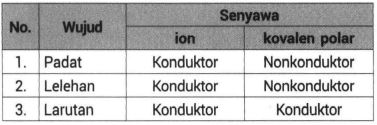
Di dalam air molekul HCl tersebut dapat terurai karena pengaruh air yang juga bersifat polar sehingga membentuk ion-ion H dan Cl -. Dalam bentuk padatan atau lelehan senyawa kovalen tidak sanggup menghantarkan lisrik alasannya yaitu molekulnya tidak mengandung ion-ion. Senyawa ion dapat menghantarkan arus listrik dalam wujud lelehan dan larutan sedangkan senyawa kovalen polar hanya menghantarkan dalam bentuk larutan senyawa kovalen nonpolar tidak dapat menghantarkan sama sekali.
Senyawa kovalen terdiri dari molekul-molekul bersifat netral dan tidak sanggup menghantarkan listrik. Pada senyawa ionik elektron diberikan dari atom dari satu unsur ke unsur lainnya. IStock Senyawa kovalen polar jika dilarutkan ke dalam air akan terurai menjadi ion-ion.
Sehingga kebanyakan senyawa kovalen ialah nonelektrolit. Terbentuknya senyawa kovalen diakibatkan oleh dua atom yang bergabung mempunyai perbedaan keelektronegatifan. Dalam bentuk padatan atau lelehan senyawa kovalen tidak dapat menghantarkan lisrik karena molekulnya tidak mengandung ion-ion.
Senyawa ion memiliki daya hantar listrik yang kuat. Senyawa Kovalen Polar Perbesar Ilustrasi senyawa kovalen dan ionik. Senyawa kovalen polar bisa menghantarkan listrik.
Perbedaan Kunci - Senyawa Ionic vs Kovalen. INI JAWABAN TERBAIK Perbedaan senyawa ion dan senyawa kovalen. Memiliki titik didih dan titik leleh yang relatif rendah.
Pada senyawa ionik elektron diberikan dari atom dari satu unsur ke unsur lainnya. Pada senyawa kovalen di samping itu elektron bersama oleh beberapa atom. Pada suhu kamar berbentuk gas ada juga yang berwujud cair dan padat.
Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas. Apabila senyawanya terionisasi sempurna maka akan dihasilkan larutan elektrolit kuat sedangkan bila senyawanya terionisasi sebagian maka akan dihasilkan larutan elektrolit lemah. Contoh zat asam misalnya hidrogen klorida HCl saat dilarutkan dalam air akan terurai menjadi ion H dan ion Cl-.
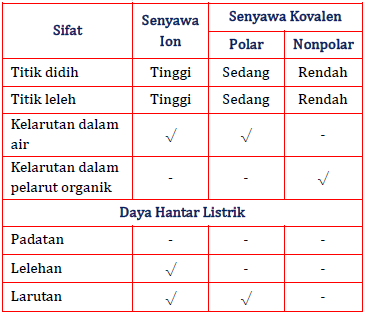
Senyawa kovalen terdiri dari molekul-molekul bersifat netral dan tidak dapat menghantarkan listrik. Perbandingan Sifat Senyawa Ion dan Kovalen Oleh karena ikatan ion dan ikatan kovalen berbeda dalam proses pembentukannya maka senyawa yang dibentuknya juga memiliki sifat-sifat fisika dan kimia yang berbedaBerikut ini akan dibahas beberapa perbedaan sifat fisika senyawa ion dan senyawa kovalen seperti kemudahan menguap volatile daya hantar listrik. Kemudahan Menguap Jika di dapur terdapat cuka senyawa kovalen dan garam dapur senyawa ion senyawa mana yang akan tercium baunya.
Lelehan NaCl dapat menghantarkan listrik dengan baik 5Isomer Tidak punya namun punya isoelektron. Senyawa kovalen polar bisa larut dalam air atau polar lain. Senyawa ion larut dalam pelarut polar 3.
Jenis ikatan yang terbentuk adalah ikatan ionik karena senyawa terbentuk dari unsur G melepas dan unsur O menerima sehingga terjadi serah terima elektron. Senyawa ion dapat menghantarkan listrik dengan baik sehingga kita dapat menggunakan dan menerapkannya dalam teknik kimia dan industri. Wujud senyawa ion pada suhu ruang biasanya adalah padat senyawa kovalen ada yang gas ada yang cair sedangkan logam biasanya padat.
Senyawa ion memiliki titik leleh yang relatif tinggi sedangkan senyawa kovalen memiliki titik leleh yang sangat rendah. Senyawa kovalen polar hanya dapat menghantarkan listrik dalam larutan dan senyawa kovalen nonpolar tidak dapat menghantarkan listrik. Tentu yang tercium adalah cuka.
Alasan utama perbedaan ini adalah perbedaan dalam pola ikatan mereka. Senyawa molekul tidak dapat menghantarkan listrik di setiap keadaan sedangkan senyawa ion jika dilarutkan dalam larutan berair dapat bertindak sebagai konduktor listrik yang baik. 6Titik Leleh dan Titik Didih.
Jadi jawaban yang benar adalah C. Oleh karena itu pola ikatan mereka dapat. Jika 12 X 24 dan 17 Y 355 berikatan maka rumus.
Ikatan ionik adalah ikatan yang dihasilkan dari perpindahan elektron dari satu atom ke atom lain. Seorang ahli kimia asal Swedia Svante August Arrhenius 1859-1927 menjelaskan asam adalah suatu zat yang ketika dilarutkan dalam air akan terurai dan menghasilkan ion H. Oleh karena itu rumus senyawa dan jenis ikatan yang terjadi adalah ionik.
Titik didih dan titik leleh senyawa logam lebih tinggi dari senyawa ion senyawa ion lebih tinggi dari senyawa kovalen. Sifat-sifat senyawa kovalen adalah. Senyawa ion memiliki sifat titik leleh yang tinggi.
Senyawa ion tidak dapat menghantarkan listrik ketika dalam keadaan padatan namun bisa menghantarkan listrik jika dilarutkan dalam pelarut polar. Berikut ini akan dibahas beberapa perbedaan sifat fisik senyawa ion dan senyawa kovalen seperti kemudahan menguap volatile daya hantar listrik dan kelarutan. Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik.
Sedangkan kovalen polar merupakan senyawa yang atom-atomnya bergabung melalui ikatan kovalen. Sedangkan senyawa kovalen memiliki sifat mudah terbakar untuk itu kita harus berhati-hati terhadap. Senyawa ion berwujud padatan berbentuk kristal.

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Pengertian Sifat Dan Contoh Dari Senyawa Ion Panduan Kimia Riset
Diketahui Data Fisik Dua Buah Senyawa Sebagai Beri
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
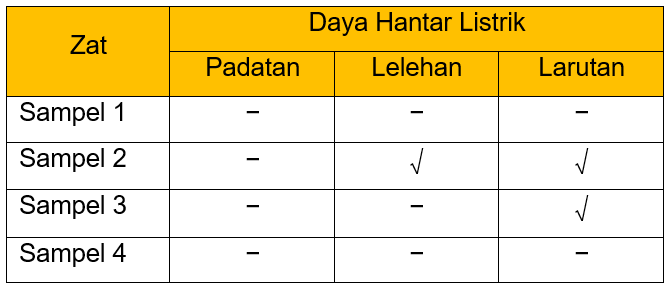
Disajikan Data Hasil Pengujian Daya Hantar Listrik

Ciri Ciri Dari Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Dalam Fase Apakah Senyawa Ion Dan Senyawa Kovalen Polar Dapat Menghantarkan Arus Listrik Jelaskan Apa Sebabnya
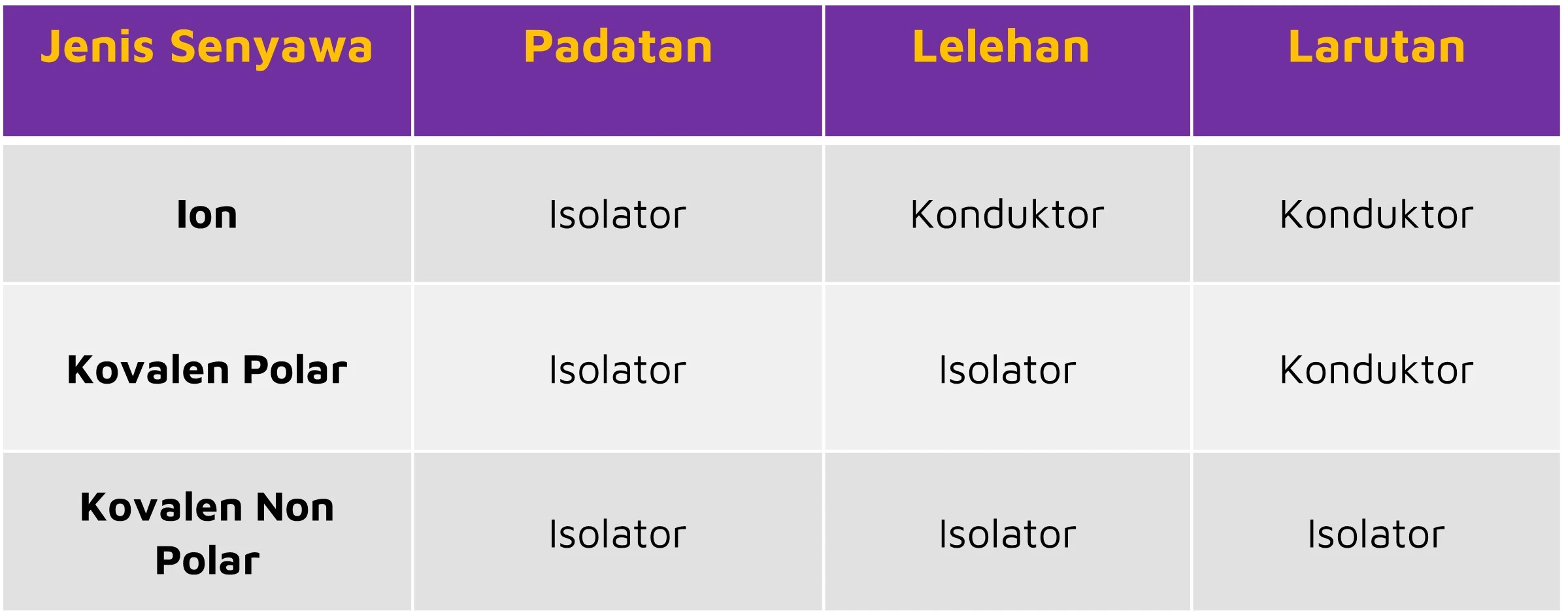
Persamaan Ionisasi Senyawa Elektrolit Dalam Air Berikut Yang Benar Adalah Duuwi Com

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Mengapa Lelehan Senyawa Kovalen Polar Tidak Dapat Menghantarkan Listrik Sedangkan Lelehan Ion Dapat Menghantarkan Listrik

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
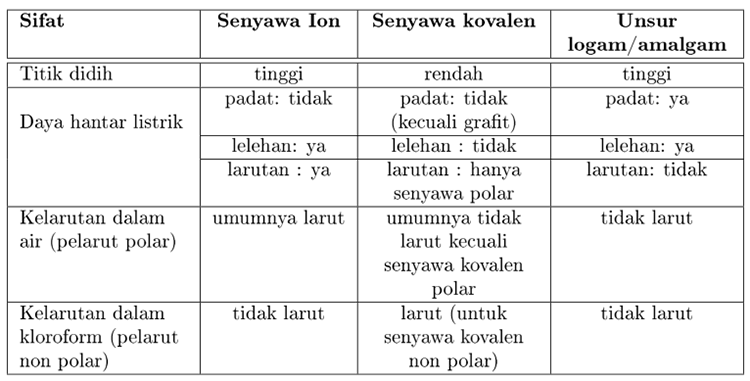
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

Fase Apakah Senyawa Ion Dan Senyawa Kovalen Polar Dapat Menghantarkan Arus Listrik

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

Sebutkan Perbedaan Sifat Antara Senyawa Ion Dengan Senyawa Kovalen Brainly Co Id

Top 10 Jelaskan Perbedaan Daya Hantar Listrik Dari Senyawa Ion Dan Senyawa Kovalen Yang Berupa Padatan 2022

Perbedaan Senyawa Ion Senyawa Kovalen Dan Lo Utakatikotak Com

